Cytomegalovirus (CMV): tác nhân nhiễm trùng có thể ảnh hưởng tất cả cơ quan trong cơ thể người
Cytomegalovirus (CMV) có thể gặp bất kỳ nơi nào trên thế giới, tồn tại khắp nơi nhiễm trùng trên người, tùy theo quần thể điều tra có thể tìm thấy tỷ lệ 40%-100% và còn thuộc vào điều kiện kinh tế xã hội; nhiễm trong trong cuộc đời sớm hơn là một đặc trưng tại các quốc gia đang phát triển, trong đó đến 50% người trẻ có huyết thanh âm tính.
Theo một số tài liệu cho thấy khoảng 80-100% dân số châu Phi, 60-70% dân số Mỹ và Tây Âu; 90-100% trẻ em và người lớn các nước đang phát triển và các nước có nền kinh tế thấp (+) với huyết thanh chẩn đoán CMV.
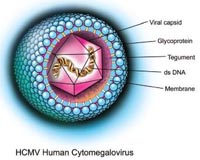
Cytomegalovirus (gốc từ Hy Lạp là cyto-, nghĩa là “tế bào” và -megalo- nghĩa là "lớn") là một giống virus được biết đến có tên thuộc họ Herpesviridae hoặc Herpesviruses. Tên virus thường viết tắt là CMV. Các loài nhiễm trên người thường được viết là human CMV (HCMV) hay human herpesvirus-5 (HHV-5), và là loại virus được nghiên cứu nhiều nhất của tất cả cytomegoloviruses. Trong nhóm Herpesviridae, CMV thuộc phụ họ Betaherpesvirinae,cũng nằm trong genera Muromegalovirus và Roseolovirus. Nó có liên quan đến các Herpesviruses khác trong phụ họ củaAlphaherpesvirinae gồm cả herpes simplex viruses (HSV-1 và - 2 và Varicella-zoster virus (VZV), và phụ họGammaherpesvirinae subfamily gồm Epstein-Barr virus. Tất cả Herpesviruses chia sẻ một đặc tính có khả năng bảo trì tiềm tàng trong cơ thể trong một thời gian dài. Mặc dù chúng có thể tìm thấy trên khắp cơ thể, nhiễm trùng CMV thường có liên quan đến tuyến nước bọt ở người và động vật Các virus CMV khác tìm thấy trên một số loài động vật có vú, nhưng các loài được phân lập từ các động vật khác với HCMV về thuật ngữ cấu trúc gen học và chưa có báo cáo gây bệnh cho người.
Cytomegalovirus (CMV) là một loại virus double-stranded DNA virus và là một thành viên của họ Herpesviridae. Theo phân loại bệnh tật quốc tế ICD 10 là B25. Các thành viên trong họ khác gồm có herpes simplex virus type 1 (HSV-1 hoặc HHV-1) và herpes simplex virus type 2 (HSV-2 hoặc HHV-2), varicella zoster virus (VZV), human herpesvirus(HHV) – 6, HHV-7, HHV-8. CMV chia sẻ nhiều sự quy kết với các loại virus herpes khác, gồm có cấu trúc bộ gen và virion và có khả năng gây ra các tình trạng nhiễm trùng tiềm tàng và trường diễn. CMV có cấu trúc bộ gen lớn nhất trong số các virus herpes. Việc sao chép có thể phân loại thành sớm ngay tức thì (immediate early), sớm trì hoãn (delayed early) và trình diện biểu hiện gen muộn (late gene expression) dựa vào thời gian tổng hợp sau khi nhiễm trùng xảy ra. DNA được sao chép bởi nhiều chu kỳ quay cuộn. HCMV chỉ phát triển ở các tế bào người và sao chép tốt nhất trên các nguyên bào sợi ở người.
Ít nhất 60% dân số Mỹ đã phơi nhiễm với CMV, với tỷ lệ hơn 90% ở trong nhóm óc nguy cơ cao (như đồng tính luyến ái ở nam giới). Tuổi dễ mắc phải tùy thuộc và khác nhau giữa các nơi trên thế giới. Tại các quốc gia đang phát triển, hầu hết nhiễm trùng mắc phải trong thời thơ ấu, ngược lại tại các quốc gia phát triển thì đến 50% người trưởng thành trẻ tuổi có kết quả huyết thanh chẩn đoán CMV âm tính.
CMV thường gây nên tình trạng nhiễm trùng không triệu chứng; tiếp sau đó là nó vẫn tồn tại một cách tiềm tàng trong cơ thể người suốt cuộc đời và có thể tái hoạt động. Nhiễm trùng được xác định khi phân lập CMV, các protein virus của chúng hoặc nucleic acid từ bất kỳ một mô nào hoặc dịch cơ thể nào. Trên các cá nhân suy giảm miễn dịch, mắc bệnh có triệu chứng thường biểu hiện như một bệnh hay hội chứng tăng bạch cầu đơn nhân (mononucleosis syndrome), lần đầu tiên mô tả trên những người trưởng thành vào năm 1965. Bệnh do CMV có ý nghĩa về mặt lâm sàng (sự tái hoạt của nhiễm trùng tiềm tàng trước đó hoặc nhiễm phải mới đây) thường phát triển trên các bệnh nhân suy giảm miễn dịch bởi nhiễm HIV, ghép các cơ quan hoặc bệnh nhân có tình trạng cấy ghép tủy xương cũng như đang dùng thuốc steroids liều cao, các thống antagonists cho hoại tử khối u, hoặc đang dùng các thuốc ức chế miễn dịch trong bệnh lý Lupus ban đỏ hệ thống (SLE), viêm khớp dạng thấp, bệnh Crohn, vảy nến.Trên các bệnh nhân đồng nhiễm với HIV, thì nhiễm trùng CMV dẫn đến tiến tới giai đoạn AIDS và thậm chí tử vong, ngay cả những người đang dùng liều thuốc chống virus sao chép ngược hoạt tính cao (highly active antiretroviral therapy_HAART).
Bệnh do CMV có triệu chứng trên các cá nhân suy giảm miễn dịch có thể ảnh hưởng đến hầu hết mỗi cơ quan trong cơ thể, dẫn đến sốt không rõ nguyê nhân, viêm phổi, viêm gan, viêm não, viêm tủy, viêm đại tràng, viêm mống mắt, kết mạc và bệnh lý thận.
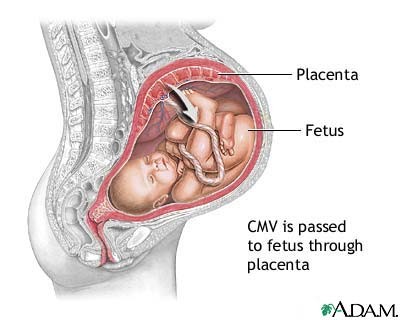
Những cá nhân có nguy cơ tăng nhiễm CMV gồm các đối tượng làm việc trong môi trường trung tâm chăm sóc, truyền máu, có nhiều bạn tình và nhiễm CMV từ việc nhận các cơ quan hoặc cấy ghép tủy xương. CMV truyền từ người sang người thông qua con đường tiếp xúc với các cá nhân đang bài tiết virus. Tác nhân gây bệnh có thể lây qua nhau thai và sữa mẹ, truyền máu và cấy ghép cơ quan. Bệnh cũng có thể lan rộng qua con đường quan hệ tình dục.
Loài virus Cytomegalovirus
Một vài loài cytomegalovirus đã được xác định và phân loại trên các động vật có vú khác nhau. Hầu hết các nghiên cứu là HCMV, điều này cũng được biết như human herpesvirus-5 (HHV-5). Các loài CMV trên các linh trưởng gồm CMV tinh tinh (chimpanzee CMV_CCMV) mà thường gây nhiễm trên các loài tinh tinh và đười ươi và loại virus trên khỉ (simian CMV_SCCMV)và trên khỉ rhesus CMV (RhCMV) nhiễm trên các khỉ đuôi dài; CCMV được xem như là cả panine herpesvirus-2 (PaHV-2) và pongine herpesvirus-4 (PoHV-4), SCCMV còn được gọi làcercopithecine herpesvirus-5 (CeHV-5) và RhCMV còn gọi là cercopithecine herpesvirus-8 (CeHV-8);
Hai loại virus nữa tìm thấy trên khỉ ban đêm (night monkey) gọi là các giống cytomegalovirus, và gọi làHerpesvirus aotus 1 và Herpesvirus aotus 3. Các loài gặm nhấm có bị nhiễm virus trước đây gọi là cytomegaloviruses mà đến hôm nay được phân loại lại theo giống muromegalovirus; giống này chứa CMV trên chuột (mouse CMV_MCMV) còn được biết với cái tên murid herpesvirus 1 (MuHV-1) và có liên quan chặt chẽ với murid herpesvirus 2 (MuHV-1) tìm thấy trên các con chuột. Ngoài ra, còn có nhiều loài virus khác có tên cytomegalovirus được xác định trên các động vật có vú khác nhau mà chúng ta vẫn chưa hiểu một cách thấu đáo về phân loại; đây là các phân lập trên chủ yếu là các loài gặm nhấm và linh trưởng.
HCMV (human cytomegalovirus)
Cytomegalovirus là một loài virus thuộc họ virus Herpesviridae hoặc Herpesviruses. Thường viết tắt là HCMVvà có thể có tên thay thế là human herpesvirus-5 (HHV-5). Trong họ Herpesviridae, HCMV thuộc họ phụBetaherpesvirinae, cũng bao gồm các Cytomegaloviruses từ các động vật có vú. Mặc dù virus được tìm thấy ở khắp nơi trên cơ thể, song nhiễm trùng HCMV thường có liên quan với tuyến nước bọt. Nhiễm HCMV điển hình thường không được chú ý trên những người khỏe mạnh, nhưng có thể đe dọa tính mạng trên các bênh nhân vốn đang bị suy giảm miễn dịch như các bệnh nhân nhiễm HIV/AIDS, cấy ghép cơ quan hoặc trẻ sơ sinh. Sau khi nhiễm HCMV,HCMV có khả năng tiềm tàng trong cơ thể trong một thời gian dài. HCMV được phát hiện trên khắp các vùng địa lý và nhóm kinh tế xã hội khác nhau và tỷ lệ nhiễm 50% và 80% trên người lớn tại Mỹ (40% trên thế giới) qua xét nghiệm phát hiện phát hiện có sự có mặt của kháng thể trong các quần thể chung như thế.
Tỷ lệ dương tính với huyết thanh là lệ thuộc vào tuổi (seroprevalence is age-dependent): 58.9% số người từ 6 tuổi trở lên nhiễm CMV trong khi đó 90.8% số cá nhân tuổi từ 80 trở lên nhiễm dương tính với HCMV. HCMV cũng là virus thường lây truyền trên các phôi thai đang phát triển. Nhiễm trùng HCMV lan rộng tại các quốc gia đang phát triển và các cộng đồng có tình hình kinh tế xã hội thấp hơn và nguyên nhân lây nhiễm virus là thường gặp có ý nghĩa trên các khuyết tật lúc sinh tại các quốc gia công nghiệp. CMV hình như có một tác động rất lớn trên các thông số về miễn dịch trong khoảng sau của đời sống và có thể góp phần làm gia tăng tỷ lệ mắc bệnh và tử vong.
Một số đặc điểm dịch tễ học
Tần suất mắc bệnh:
- Tại Mỹ:
Nhiễm trùng CMV được xem là rất đặc biệt với con người. Tuổi và đặc điểm lâm sàng cũng như đường lây truyền có thể khác nhau từ người này sang người khác, nhưng một vài người đã thoát khỏi nhiễm trùng trong cuộc đời của họ.
- Trên thế giới:
Các điều tra về huyết thanh học tiến hành trên khắp thế giới chỉ ra CMV tồn tại khắp nơi nhiễm trùng trên người. Lệ thuộc vào quần thể điều tra, CMV có thể tìm thấy với tỷ lệ 40%-100% trong quần thể và còn thuộc vào điều kiện kinh tế xã hội. Nhiễm trong trong cuộc đời sớm hơn là một đặc trưng tại các quốc gia đang phát triển, ngược lại có đến 50% người trẻ có huyết thanh âm tính tại nhiều quốc gia phát triển.
Bệnh có thể gặp bất kỳ nơi nào trên thế giới. Theo một số tài liệu cho thấy khoảng 80-100% dân số châu Phi, 60-70% dân số Mỹ và Tây Âu; 90-100% trẻ em và người lớn các nước đang phát triển và các nước có nền kinh tế thấp (+) với huyết thanh chẩn đoán CMV.
Tại Việt Nam, chưa có công trình nghiên cứu nào nói về tỷ lệ nhiễm CMV.
Tỷ lệ mắc bệnh / tử vong
CMV hiếm khi liên quan đến tỷ lệ tử vong trên các cá nhân có miễn dịch (< 1%). Tỷ lệ mắc bệnh có thể xảy ra trên các bệnh nhân có hội chứng bệnh đơn nhân đã được mô tả trên các ca bệnh nhiễm trùng CMV ở người lớn có miễn dịch bình thường..
Các người nhận ghép cơ quan đặc hoặc tủy xương, CMV có thể gây ra tỷ lệ tử vong và mắc bệnh đáng lưu ý. Chẳng hạn, ngay cả khi dùng liệu pháp chống virus, tỷ lệ tử vong trên các người nhận ghép tủy đồng loại có viêm phổi kẻ dao động từ 15%-75%.
Phương thức lây truyền:
Đường miệng và đường hô hấp là đường lây nhiễm CMV nổi bật nhất. Ngoài ra, CMV còn lây truyền từ người sang người qua nước bọt, nước tiểu, tinh dịch, sửa, dịch tiết của tử cung âm đạo;
Truyền máu, ghép phủ tạng của người nhiễm CMV;
Quan hệ tình dục với người nhiễm CMV cũng là đường lây truyền đặc biệt quan tâm.
Tuổi:
Tỷ lệ mắc bệnh CMV tăng theo tuổi. Tuổi cũng là yếu tố nguy cơ cho bệnh nhiễm CMV trong một số quần thể có cấy ghép cơ quan.
Tại Mỹ, lây truyền hay bệnh do CMV bẩm sinh từ một bà mẹ đang nhiễm trùng cấp trong quá trình mang thai là một nguyên nhân quan trọng gây các bất thường về thần kinh và điếc khoảng 8000 đứa trẻ sinh ra mỗi năm.Các chủng khác biệt về mặt di truyền của virus CMV. Sự khác biệt về mặt kiểu gen có thể liên quan với sự khác nhau về mặt độc lực. Nhiễm trùng nhiều hơn một chủng CMV có thể tìm thấy trên một số người cấy ghép cơ quan. Nhiễm đôi là một vấn đề có thể giải thích cho bệnh CMV bẩm sinh ở các trẻ em có các bà mẹ có CMV dương tính.
Chưa có tài liệu nào nghiên cứu về phân bố thời gian nhiễm CMV cụ thể.
Sinh lý bệnh học
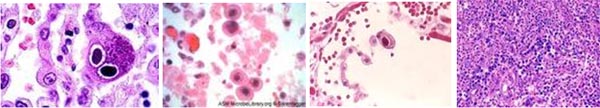
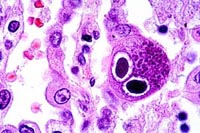
CMV là một loại virus ly giải (lytic virus) có thể gây nên các hiệu ứng tác động cytopathic trên in vitro và in vivo. Điểm đặc trưng về bệnh học nhiễm trùng CMV là tế bào trương phình với các tiểu thể, kể cả virus. Các tế bào biểu hiện lớn, trương phình cũng đã được nhìn thấy trong các ca bệnh nhiễm trùng bởi các virus khác thuộcBetaherpesvirinae. Đặc điểm vi thể cho thấy các tế bàonày là hình ảnh hay gặp nhất là mắt cú (“owl's eye”). Mặc dù vấn đề chẩn đoán đã được cảnh giác và cân nhắc, song các xét nghiệm mô học như thế có thể gặp ở các cơ quan nhiễm trùng có hoặc không.
Khi vật chủ bị nhiễm, CMV DNA có thể được phát hiện bằng phản ứng PCR trong tất cả các cầu nối liên kết tế bào khác nhau. Dưa vào nhiễm trùng ban đầu, CMV nhiễm vào các tế bào biểu mô của tuyến nước bọt, nhiễm trùng dai dẳng và ẩn chứa virus bên trong nó. Nhiễm trùng hệ tiết niệu dẫn đến các sự tồn lưu virus không biểu hiện lâm sàng. Mặc dù sự sao chép virus vẫn đang diễn ra trong thận, thì rối loạn chức năng thận hiếm khi xảy ra ngoại trừ trên người nhận các tạng ghép, trên những đối tượng đó CMV có liên quan đến các ca bệnh lý cầu thận và khả năng đào thải mảnh ghép là có thể.
Miễn dịch học
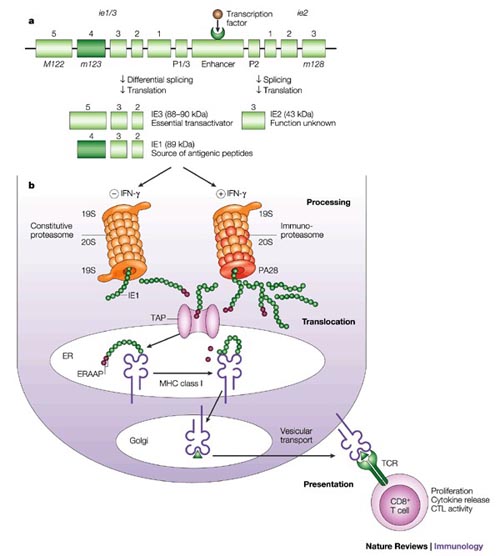
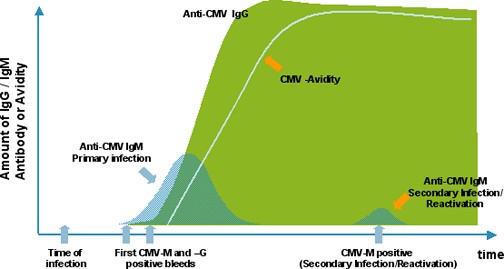
Nhiễm trùng CMV tiên phát được xác định khi nhiễm trùng trên một cá nhân trước đó phải xác định có huyết thanh chẩn đoán âm tinh với CMV. Trên các bệnh nhân này, các kháng thể CMV immunoglobulin M (IgM) có thể tìm thấy rất sớm 4-7 tuần sau khi nhiễm trùng ban đầu và có thể tồn tại kéo dài 16-20 tuần. Hầu hết các kháng thể trung hòa đều trực tiếp chống lại lớp vỏ bọc của glycoprotein gB. Các nghiên cứu chỉ ra có hơn 50% hoạt tính trung hòa với huyết thanh trung tính có liên quan đến glycoprotein gB. Tuy nhiên, các protein cấu trúc vi vỏ của virion như pp150, pp28 và pp65 biểu hiện mạnh và đáp ứng kháng thể bền vững.
CMV là một virus có tình điều hòa miễn dịch (immunomodulatory virus) và có thể làm nặng thêm một tình trạng bệnh lýmiễn dịch sẵn có (như bệnh lupus ban đỏ). CMV DNA trong máu và virus trong máu thường tìm thấy trên các cá nhân khỏe mạnh phụ nữ có CMV (+). Miễn dịch do mắc phải tự nhiên đối với virus dường như không ngăn ngừa được sự tái nhiễm hoặc quá trình virus ẩn mình trong cơ thể. Miễn dịch qua trung gian tế bào được xem là yếu tố quan trọng nhất trong việc chống lại nhiễm virus CMV. Các bệnh nhân thiếu hụt miễn dịch qua trung gian tế bào có nguy cơ cao nhất đối với bệnh do CMV. Các tế bào lymphocyte đặc hiệu CD4+ và CD8+ đóng vai trò quan trọng trong bảo vệ miễn dịch sau nhiễm tiên phát hoặc sự tái hoạt của một bệnh lý đang tiềm tàng. Các nghiên cứ về những người ghép tủy xương cho thấy không hìn thành và phát triển lên các tế bào CD4+ hoặc CD8+ đặc hiệu cho CMV đối với nhóm nguy cơ cao nhất viêm phổi do CMV. Bên cạnh đó, không có trường hợp nào viêm phổi do CMV đã được báo cáo trên những cá nhân ghép tủy đồng loại nhận truyền tế vào CD8+ đặc hiệu với virus CMV.
Nhiễm trùng CMV tiên phát và tình trạng có virus trong máu (viremia)
Trong hầu hết các vật chủ, nhiễm trùng tiên phát CMV có triệu chứng lâm sàng rất yên lặng. Triệu chứng lâm sàng các nhiễm trùng tiên phát trên các ca bệnh người lớn nhiễm CMV trên các đối tượng có miễn dịch tốt. Nhiễm trùng CMV trên các bệnh nhân suy giảm miễn dịch mang nguy cơ cao nhất đối với bệnh CMV.
Tình trạng nhiễm virus trong máu được chẩn đoán nhờ vào phân lập CMV trên nuôi cấy (hoặc là thông qua nuôi cấy chuẩn (standard or shell vial culture), các chất tiết CMV trong nước botjh và nước tiểu là thường xảy ra trên các bệnh nhân suy giảm miễn dịch và nói chung có ít hậu quả. Ngược lại, tồn tại virus trong các tạng nhận ghép được xem là nguy cơ cao nhất đối với bệnh nhiễm CMV. Độ nhạy của phát hiện virus trong máu của CMV như là một chỉ điểm (marker) phát hiện viêm phổi do CMV là 60 -70% trên các người ghép tủy xương đồng loài (allogeneic marrow transplant). Không có bằng chứng virus trong máu có một giá trị tiên đoán âm tính cao đối với bệnh CMV. Liệu pháp dùng thuốc virus dự phòng và điều trị ngăn chặn chống lại bệnh CMV trên các bệnh nhân có cấy ghép tạng điển hình dựa vào phát hiện CMV trong máu thông qua nuôi cấy, kháng nguyên CMV trong máu và kỹ thuật PCR.
Bệnh do CMV bẩm sinh (CCMD_Congenital cytomegalovirus disease)
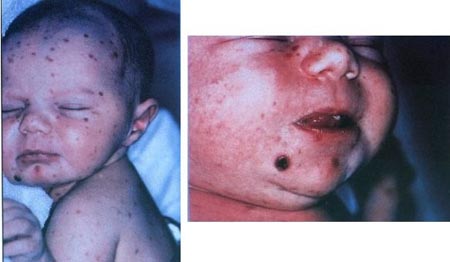
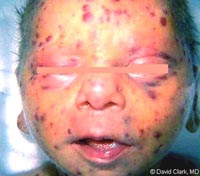
Nhiễm trùng CMV bẩm sinh là một trong những nguyê nhân dẫn đến hội chứng nhiễm trùng TORCH (toxoplasmosis, other infections including syphilis, rubella, CMV, HSV), mang các nguy cơ khác nhau gây các bệnh lý có ý nghĩa quan trọng và các khuyết tật sơ sinh. Hội chứng lâm sàng của bệnh do CMV bẩm sinh bao gồm vàng da, gan lách to, giảm tiểu cầu, chậm phát triển trong tử cung, tật đầu nhỏ và viêm võng mạc.
Đặc điểm lâm sàng thường gặp nhất trong thể CMV bẩm sinh là gồm chấm xuất huyết (71%), vàng da (67%), tật đầu nhỏ (53%) và tuổi thai so với thai nhỏ rất nhiều (50%). Một số bất thường về cận lâm sàng hay thấy là tăng bilirubine máu (81%), tăng các men gan (83%), giảm tiểu cầu (77%) và tăng nồng độ protein trong dịch não tủy (77%). Các nghiên cứu chỉ ra trên các trẻ em không có triệu chứng biểu hiện thần kinh và có thể có phát hiện kháng thể IgM của CMV. Nhiểu trường hợp mất thính giác trên các trẻ em do nhiễm trùng CMV. Sự bài tiết CMV là một tình trạng hay gặp trên trẻ em, nhiễm trùng bẩm sinh và có thể biểu hiện như một ổ chứa cho các trẻ em khác và những người chăm sóc trẻ.
Tình trạng miễn dịch CMV của phụ nữ xác định là nguy cơ nhiễm trùng nhau thai và có triệu chứng tiếp sau đó trên các trẻ em hoặc bào thai. Bệnh do CMV bẩm sinh có triệu chứng hiếm khi xảy ra trên các phụ nữ có đáp ứng miễn dịch tồn tại trước đó hơn là các cá nhân chưa bao giờ có miễn dịch đối với CMV. 1/10 số ca nhiễm CMV cấp tính trong thời gian mang thai là nghi ngờ có khả năng dẫn đến tình trạng bệnh CMV bẩm sinh.
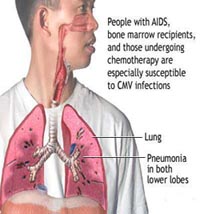
Viêm phổi do CMV (Cytomegalovirus pneumonia)
Viêm phổi do CMV được xác định khi có dấu chứng và triệu chứng của bệnh phổi khi có phối hợp với phát hiện kháng nguyên CMV trong dịch phế quản-phế nang hoặc nhu mô phổi. Phát hiện CMV nên được thực hiện thông qua nuôi cấy, nghiên cứu mô học bệnh và phân tích hóa mô miễm dịch hoặc kỹ thuật lai tại chỗ vì phương pháp PCR phát hiện hoặc chẩn đoán CMV DNA đơn thuần quá nhạy để chẩn đoán viêm phổi CMV.
Khoảng 0-6% người trưởng thành nhiễm CMV như là một hội chứng bạch cầu đơn nhân phát triển lên viêm phổi. Một nghiên cứu tìm thấy tỷ lệ mắc mới của viêm phổi do CMV trên các bệnh nhân có suy giảm miễn dịch là 19%. Trong hầu hết ca ca bệnh, viêm phổi do CMV tìm thấy qua chụp xX - quang phổi và không có ý nghĩa lâm sàng, giải quyết nhanh chóng với sự biến mất nhiễm trùng tiên phát.
Viêm phổi do CMV đe dọa tính mạng có thể hình thành trên các bệnh nhân suy giảm miễn dịch. Tỷ lệ cao nhất của viêm phổi do CMV, cũng như độ nặng cao nhất, xảy ra trên các bệnh nhân ghép phổi – là nhóm đối tượng có toàn bộ > 50% của ca bệnh CMV đang phát hiện (nhiễm trùng hay bệnh).
Viêm gan do virus CMV (Cytomegalovirus hepatitis)
Viêm gan do virus CMV được xác định khi có nồng độ bilirubin và / hoặc các men gan tăng cao cùng với phát hiện có CMV mà không tìm thấy sự phối hợp với các nguyên nhân hoặc tác nhân khác gây viêm gan. CMV có thể phát hiện thông qua nuôi cấy, làm mô bệnh học, hóa mô miễn dịch hoặc lai tại chỗ. Phản ứng PCR phát hiện CMV dùng để chẩn đoán dường như chưa thỏa đáng, vì kết quả dương tính có thể phản ánh tình trạng xuất hiện virus thoáng qua. Ca bệnh đầu tiên viêm gan do virus CMV liên quan đến một trẻ em bị viêm kết mạc và màng mạch nho, gan lách to và có sự calci hóa ở não.
Viêm gan thường thấy trên các bệnh nhân nhiễm trùng CMV tiên phát và bệnh bạch cầu đơn nhân. Nồng độ các enzyme tế bào gan có thể tăng nhẹ và thoáng qua, trong một trường hợp hiếm có thể gặp vàng da. Tiên lượng bệnh nhân viêm gan do virus CMV trên các cá nhân suy giảm miễn dịch chưa rõ ràng, nhưng tử vong đã được báo cáo. Xét nghiệm về mô học điển hình cho thấy sự thâm nhiễm các tế bào đơn nhân ở vùng tĩnh mạch cửa nhưng cũng có thể có quá trình viêm sinh u hạt.
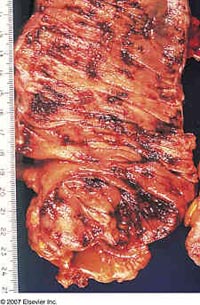
Viêm dạ dày và đại tràng do CMV (Cytomegalovirus gastritis and colitis)
Bệnh do CMV ở đường tiêu hóa được xác định khi có sự phối hợp các triệu chứng của đường tiêu hóa trên và tiêu hóa dưới, tổn thương niêm mạc có thể nhìn thấy quá nội soi và phát hiện CMV thông qua nuôi cấy, xét nghiệm mô học và xét nghiệm hóa mô miễn dịch và lai tại chỗ. Viêm đại tràng do CMV được báo cáo lần đầu tiên vào năm 1985 trên hai người đàn ông đồng tính luyến ái có biểu hiện đau bụng, tiêu chảy, đi tiểu ra máu (hematochezia). Làm kỹ thuật PCR đơn thuận xét nghiệm CMV không đủ để chẩn đoán vì kết quả dương tính có thể phản ánh sự lưu lại virus thoáng qua mà thội.
CMV có thể nhiễm vào đường tiêu hóa từ khoang miệng qua con đường đại tràng. Đặc điểm lâm sàng điển hình của bệnh là tình trạng tổn thương dạng loét. Trong khoang miệng, các thương tổn này có thể phân biệt với các vết loét do HSV hoặc loét aphthous. Viêm dạ dày có thể đau bụng và thậm chí nôn ra máu, ngược lại viêm đại tràng thường biểu hiện một bệnh lý tiêu chảy nhiều hơn. Bệnh do CMV ở đường tiêu hóa thường sống ngắn hơn so với các cơ quan khác vì thường bị suy sụp ở các tế bào nhiễm trên niêm mạc tiêu hóa.
Bệnh do CMV ở hệ thần kinh trung ương (Cytomegalovirus CNS disease)
CMV ở hệ thần kinh trung ương xác định khi có triệu chứng thần kinh trung ương kèm theo sự phối hợp phát hiện ra CMV trong nước tiểu (nuôi cấy, PCR) hoặc sinh thiết mô não nuôi cấy, hóa mô miễn dịch và lai).
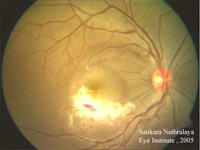
Viêm võng mạc do CMV (Cytomegalovirus retinitis)
Viêm võng mạc do CMV là một trong những nhiễm trùng ocw hội hay gặp nhất trên các bệnh nhân AIDS, điển hình đặc trưng là có CD4+ lymphocyte < 50 tế bào/µL. Dù số lượng ca bệnh giảm khi sử dụng phác đồ HAART, nhưng các ca mới vẫn tiếp
tục báo cáo. Các cá nhân nhiễm CMV viêm võng mạc cho hình ảnh giảm tiến triển về thị lực, có thể diễn tiến đến mù nếu không điều trị. Bệnh có thể biểu hiện một bệnh cũng có thể hai bên. Điều trị CMV thường kéo dài để ngăn ngừa tái phát viêm võng mạc do CMV. Tất cả tổn thương nghi ngờ viêm võng mạc do CMV phải xác định nhờ vào các nhà nhãn khoa.
Hội chứng tái hồi phục lại miễn dịch (Immune reconstitution syndrome_IRIS) được báo cáo trong số 16%-63% trường hợp bệnh nhân nhiễm HIV có viêm võng mạc do CMV theo sau liệu trình HAART. Trong một nghiên cứu, thời gian trung bình đối với IRIS sau khi HAART dùng là 43 tuần nhưng cũng đã có báo cáo sớm 4 tuần và muộn đến 4 năm trên một số trường hợp. CMV IRIS có thể biểu hiện “floater” từng đợt không đau, sợ ánh sáng, giảm thị lực, đau nhãn cầu. Một số bệnh nhân có phù điểm vàng dẫn đến mất thị lực hoặc bệnh lý màng mạch nho và võng mạc tăng sinh, xuất huyết màng mạch nho tự phát và bong võng mạc.
Viêm thận do CMV (Cytomegalovirus nephritis)
Viêm thận do CMV xác định khi phát hiện có sự phối hợp với sinh thiết thận chỉ ra có sự thay đổi liên quan đến CMV trên các bệnh nhân suy thận. Làm PCR đối với CMV không đủ chẩn đoán, đáng chú ý là việc phát hiện CMV trong nước tiểu bệnh nhân suy thận không hội đủ tiêu chuẩn chẩn đoán đối với trường hợp là viêm thận do CMV. Tồn tại CMV trong máu có liên quan đến tổn thương cầu thận cấp.
Hội chứng do nhiễm virus Cytomegalovirus
Nói chung, điều tốt nhất để tránh tình trạng các đối tượng được cấy ghép tế bào như các virus khác (HHV-6) cũng có thể gây sốt và ức chế tủy xương. Tuy nhiên, cấy ghép các cơ quan đặc, hội chứng CMV sẽ đươc xác định tốt hơn: sốt (> 38°C) ít nhất 2 ngày trong giai đoạn 4 ngày, phát hiện CMV trong máu hoặc có giảm bạch cầu đa nhân trung tinh và tiểu cầu.
Ghép mô hoặc mảnh ghép và bệnh của vật chủ
Nhiễm trùng CMV có liên quan đến ghép cấp trên các bênh nhân ghép tủy xương. Đa kiểu gen (gB 1-4) của CMV tồn tại, mỗi sự hác biệt trong gen mã hóa lớp vỏ bọc của glycoprotein gB. Liên quan giữa gB types với vật chủ ghép cấp và tử vong liên quan đến ức chế tủy đã được kiểm tra. Liên quan đến loại bệnh này, sự hài hòa và thống nhất của hệ kháng nguyên HLA giữa người cho và nhận, tình trạng huyết thanh CMV của người cho, tuổi (Torok-Storb và cs.,1997) tìm thấy rằng gB3 và gB4 liên kết hoặc liên quan với mức độ ức chế tủy xương và tử vong cao.Điều thú vị, không có kiểu gen CMV đặc hiệu nào liên kết với hậu quả xấu với người ghép các cơ quan đặc, mặc dù nhiễm tr4ungf phải kiểu gen hỗn hợp mixed gB genotype có liên quan đến lượng virus cao hơn và quá trình làm sạch virus chậm.
Đặc điểm lâm sàng
Bệnh sử và diễn tiến bệnh trên lâm sàng cũng như xét nghiệm lệ thộc vào tình trạng miễn dịch của bệnh nhân còn tốt hoặc đã suy giảm nặng:
Nhiễm trùng CMV trên các cá nhân còn hệ thống miễn dịch ở người lớn
Cytomegalovirus (CMV) có thể gây ra một loạt nhiễm trùng trên các bệnh nhân có hệ miễn dịch. Vị trí hay liên quan đến nhiễm virus này bao gồm phổi (viêm phổi virus mắc phải cộng đồng nặng), gan (transaminitis), lách (lách lớn), đường tiêu hóa (viêm đại tràng), thần kinh trung ượng (viêm não), hệ thống huyết học (giảm tế bào máu) và liên quan đến đa cơ quan (sốt không rõ nguyên nhân). Các vị trí không thường gặp của nhiễm trùng CMV trên các cá nhân miễn dịch gồm thận, tuyến adrenal, tuyến nước bọt, tụy và thực quản.
Trong hầu hết các trường hợp, nhiễm trùng CMV tiên phát là không có triệu chứng hoặc chỉ có các triệu nhẹ giống cúm. Trường hợp có triệu chứng, khi xuất hiện sẽ hình thành 9-60 ngày sau khi nhiễm đầu tiên. Các hạch lympho và lách có thể to lên, vì thế nhiễm trùng CMV nên đưa vào chẩn đoán phân biệt với các bệnh nhiễm trùng khác có sinh các triệu chứng bệnh lý hạch lympho. Suy nhược trầm trọng có thể tồn tại ngay cả sau khi xét nghiệm trở về bình thường.
CMV có thể sinh ra hội chứng tăng bạch cầu đơn nhân tương tự như khi nhiễm virus Epstein-Barr virus(EBV), bệnh toxoplasmosis tiên phát, hoặc đảo ngược huyết thanh HIV cấp. Cả virus CMV và EBV có thể dẫn đến tăng bạch cầu lympho không điển hình trong máu. Các kết quả thích hợp của xét nghiệm khác gồm nghiên cứu kháng thể heterophil âm tính, tăng nhẹ hoặc vừa men aspartate aminotransferases và có bằng chứng tan huyết chưa biểu hiện lâm sàng (subclinical hemolysis). Viêm gan và tăng lymphocyte không điển hình biến mất sau 6 tuần. Mặc dù độ nhạy của nó lớn, song xét nghiệm CMV IgM có giới hạn do phản ứng chéo với nhiễm trùng EBV cấp khi có huyết thanh biểu hiện tăng bạch cầu đơn nhân. Phản ứng dương tính giả có thể do các yếu tố thấp (rheumatoid factors).
Nhiễm trùng CMV nên được xem xét trên những bệnh nhân có tăng bạch cầu đơn nhân nhiễm trùng hoặc sốt không rõ nguyên nhân. Hầu hết các ca có ít biểu hiện về mặt thực thể. Một số nghiên cứu chỉ ra rằng khi một nhóm bệnh nhân nhiễm CMV ít có lách lớn, gan lớn và viêm hầu họng hơn là bệnh nhân nhiễm EBV. Các bệnh nhân nhiễm bạch cầu đơn nhân có CMV có thể lớn hơn, thời gian sốt dài hơn và hạch cổ ít hơn. Tuy nhiên, các triệu chứng lâm sàng như thế không đủ phân biệt giữa 2 loại nhiễm virus này.
Truyền nhiều đơn vị máu cũng là một nguy cơ cho bệnh tăng bạch cầu đơn nhân CMV và rất phức tạp trong các trường hợ sốt sau mổ hoặc sốt trên các bệnh nhân sau chấn thương. Về kinh điển, test kháng thể với CMV thực hiện sử dụng phản ứng cố định bổ thể chỉ ra hiệu giá kháng thể virus đỉnh là ở thời điểm 4-7 tuần sau khi nhiễm. Nhiều test thực hiện phát hiện kháng thể CMV giờ đây có sẵn, một số đó nhạy đủ phát hiện kháng thể anti-CMV IgM sớm trong quá trình bệnh và trong suốt quá trình tái hoạt CMV. Sự tái hoạt virus không thường xảy ra, đôi khi xảy ra dạng virus trong máu và kết quả IgM (+) với sự có mặt kháng thể IgG (+). Điều này thường thấy trong các trường hợp nhiễm từng đợt hoặc vào lúc có sang chấn ở bệnh nhân. Ý nghĩa lâm sàng, thời gian bệnh và bệnh sử trên những bệnh nhân suy giảm miễn dịch chưa được thấu đáo liên quan đến virus.
Trên một số trường hợ hiếm gặp, CMV có thể gây viêm phỏi mắc phải trong cộng đồng ở nhưng cá nhân có miễn dịch cần xem xét như là một tác nhân có thể (cùng với cúm [người, heo, chim] và adenovirus) trên một số ca viêm phổi mắc phải do virus nặng. Báo cáo ca bệnh mô tả sốt kéo dài, không có triệu chứng ho và dấu chứng hô hấp khác, thâm nhiễm từng đám hoặc viêm phổi kẻ hai bên trên phim chụp X-quang phổi, giảm lymphocyte tương đối, tăng lymphocyte không điển hình và tăng các men transaminase. Đáng chú ý, một số bệnh nhân có kháng thể CMV IgM (-) nhưng sau đó lại tăng cả IgM và IgG, giải quyết triệu chứng thâm nhiễm qua 6 tuần. Có nhiều mức độ thiếu khí khác nhau. Tiên lượng viêm phổi do CMV khác nhau trên các bệnh nhân có miễn dịch, ngay cả ca nặng thường là tốt, hiếm khi đòi hỏi liều trình điều trị virus đầy đủ và thường khỏi.
Đặc điểm lâm sàng hiếm hơn của nhiễm trùng CMV trên các bệnh nhân miễn dịch gồm có hội chứng Guillain-Barré, viêm nao-màng não, viêm màng ngoài tim, viêm cơ tim, giảm tiểu cầu và thiếu máu tan máu. Các ban đỏ dạng sốt phát ban rubella (Rubelliform) hoặc mảng tấm lồi lên (maculopapular rashe) là các hình thái cũng gặp có hoặc không có chỉ định dùng Ampicillin. Loét tiêu hóa có thể dẫn đến từ nhiễm trùng CMV cấp trên những đối tượng miễn dịch, dù các dấu này có thể giống như các cá nhân suy giảm miễn dịch.
Nhiễm trùng CMV trên các đối tượng đặc biệt
Nhiễm trùng CMV trên các đối tượng suy giảm miễn dịch
Nhiễm trùng CMV trên các cá nhân ghép tạng có thể tiên phát cũng óc thể là tái nhiễm. có thể xét nghiemj dương tính CMV trên những cá nhân trước đó âm tính với CMV, trong khi nhiễm trùng tái nhiễm gồm cả sự tái nhiễm hay nhiễm mới (reinfection) và tái hoạt (reactivation). Tái nhiễm ám chỉ đến phát hiện một chủng CMV khác với chủng đã gây ra trên gây ra nhiễm trùng ban đầu ở bệnh nhân đó. Sự tái hoạt được xác định khi nhiễm với cùng chủng CMV đã nhiễm trước đó.
Nhiễm trùng CMV có thể gây nên các tác động trực tiếp hoặc gián tiếp. Các tác động trực tiếp gồm có ức chế tủy xương, viêm phổi, bệnh đường tiêu hóa, viêm cơ tim, bệnh đường tiêu hóa, viêm gan, viêm tụy, viêm thận, viêm võng mạc và viêm não. Các ảnh hưởng gián tiếp chính gồm có đào thải mảnh ghép cấp tính hoặc mạn tính, xơ vữa động mạch vành tim tăng lên, nhiễm trùng nấm hoặc vi khuẩn thứ phát, bệnh lý tăng sinh lympho bào sau ghép có liên quan đến EBV (EBV-associated posttransplant lymphoproliferative disease_PTLD) và giảm mảnh ghép cũng như mức độ sống còn của bệnh nhân. Nhiễm trùng CMV có thể ảnh hưởng lên cùng một hệ thống cơ quan ở các bệnh nhân nhiễm HIV (+) có chỉ số CD4 thấp trên các bệnh nhân cấy ghép cơ quan. Viêm võng mạc đã được báo cáo như là bệnh chính ucar CMV với HIV, sau đó có liên quan đến thần kinh trung ương.
Không khỏi ngạc nhiên, bệnh do CMV có liên quan đến giảm sự sống còn của bệnh nhân ghép tạng. Một ví dụ cho thấy, trong một nhóm người gồm 187 bệnh nhân ghép phổi tại Thụy Điển từ năm 1990 và 2002, tỷ lệ sống sót 10 năm chỉ 32% trên các bệnh nhân có kèm theo nhiễm trùng CMV, so với nhóm nhiễm trùng CMV không triệu chứng là 53% và không nhiễm trùng CMV là 57%.
Cấy ghép cơ quan và nhiễm Cytomegalovirus
CMV là một trong những tác nhân gây bệnh quan trọng được phân lập trên một cơ quan ghép ở người như một nhiễm trùng tiên phát CMV, và có thể biểu hiện nặng. Bệnh do CMV xảy ra với tần suất cáo nhất trên các đối tượng ghép tạng. Mối liên quan này là có thật đối với tất cả cơ quan ghép ngoại trừ người ghép tủy xương, ở đó có tỷ lệ mắc mới CMV cao. Lý do giải thích vì sao như vậy đến nay chưa rõ nhưng có thể liên quan đến mức độ ức chế miễn dịch do ddieuf trị và quá trình ghép và chống thải ghép mang lại.
Những bệnh nhân cấu ghép tủy xương chịu điều trị hóa liệu pháp cách công cụ “ablative chemotherapy” và tia xạ. Một giai đoạn giảm bạch cầu và mất hoạt tính kháng nguyên đặc hiệu sau đó. Tất cả người ghép có một giai đoạn giảm miễn dịch qua trung gian tế bào đặc hiệu với CMV. Bước tiếp theo chưa biết, tuy nhiên, các bệnh nhân có nguy cơ lớn nhất đối với bệnh CMV đã có virus trong máu. Virus trong máu đóng một vai trò trong cơ chế sinh lý bệnh của bệnh CMV đến nay vẫn chưa rõ ràng.
Viêm phổi do CMV đe dọa tính mạng có thể tiến triển trên các bệnh nhân suy giảm miễn dịch, với tỷ lệ mắc thay đổi tùy theo loại tạng ghép. Các bệnh nhân ghép tủy xương, gan, phổi, tim, thận tụy có mức độ ức chế miễn dịch khác nhau. Hầu hết nguy cơ gồm người ghép tủy và phổi. Trên các bệnh nhân ghép tủy xương, bệnh do CMV hầu như có mắt sau khoảng 30-60 ngày kể từ khi ghép. Viêm phổi tử vong do CMV ích gặp hơn các bệnh nhân ghép các tạng đặc khác. Các bệnh nhân này dù ban đầu thâm nhiễm trên phim chụp x quang nhưng không có triệu chứng.
Trình bày lâm sàng hay gặp nhất của viêm phổi do CMV là sốt, khó thở kèm theo thâm nhiễm kẻ. Chẩn đóan phân biệt của viêm phổi CMV trên các bệnh nhân suy giảm miễn dịch gồm có viêm phổi do Pneumocystis carinii, nhiễm trùng hô hấp do virus, xuất huyết phổi, nhiễm độc thuốc, u lumpho tái phát và các loại nhiễm trùng khác. CMV thường được phát hiện trên phổi các bệnh hân nhiễm HIV/AIDS nhưng lại thường biểu hiện chứa virus và không gây ý nghĩa lâm sàng của bệnh.
Viêm phổi do CMV khó điều trị, ngay cả khi thuốc chóng virus đã sẵn có. Tỷ lệ tử vong trong số các đối tượng ghép tủy có viêm phổi do CMV khoảng 85% trước khi cho dùng Ganciclovir và CMV-specific immune globulin. Bên cạnh các thuốc này đã làm giảm đi tỷ lệ tử vong viêm phổi do CMV 15%-75%. Tỷ lệ tử vong do viêm phổi trên các bệnh nhân ghép tủy xương đòi hỏi phải thông khí can thiệp kèm theo điều trị Ganciclovir và immune globulin. Hiệu quả lâm sàng nghèo nàn cũng thấy trên các bệnh nhân nhiễm virus hô hấp cộng đồng (như parainfluenza, influenza, virus hợp bào đường hô hấp và những người ngày ghép tủy đồng loại. Đề nghị này cho thấy độ nặng của viêm phổi CMV.
Sử dụng immune globulin dựa trên các nghiên cứu của người ghép tủy, đáng chú ý tỷ lệ sống sót cải thiện khi dùng liệu pháp chống virus trên các bệnh nhân viêm phổi CMV (ganciclovir plus immune globulin). Điều này chưa được nghiên cứu trên các bệnh nhân viêm phổi do CMV có ghép các tạng đặc. Mọt số chuyên gia tin rằng cơ chế viêm phổi do CMV trên các bệnh nhân ghép tạng đặc khác với ghép tủy xương, cho immune globulin không cần thiết. Viêm phổi trên các đối tượng ghép tủy xương không liên quan đến hiệu ứng virus trực tiếp trên các tế bào phổi. Bổ sung các CMV-specific immune globulin chưa cho thấy ảnh hưởng lên tỷ lệ mắc bệnh và tỷ lệ tử vongcủa nhiễm CMV với các cơ quan khác;
Bệnh CMV nặng có thứ phát sau khi cùng với nhiễm virus và các yếu tố khác như tia xạ, hóa liệu pháp, đáp ứng viêm không miễn dịch hoặc nhiễm trùng khác. Chẩn đoán viêm phổi CMV lệ thuộc vào sự hồi phục CMV từ các bệnh nhân có kết quả chụp x quang dương tính phù hợp với triệu chứng trên lâm sàng. CMV có thể phân lập từ phổi thông qua dịch rửa phế quản và tiểu phế quản (bronchoalveolar lavage_BAL) hoặc sinh thiết phổi hở.
Để hỗ trợ chẩn đoán, kháng nguyên CMV tìm thấy trên các bệnh phẩm mô bệnh học. CMV phân lập trên các mẫu bệnh phẩm lâm sàng khi không có triệu chứng lâm sàng có thể virus đang sao chép ở giai đoạn tiền lâm sàng. Trong nhiều trường hợp, việc phát hiện các sao chép tiền lâm sàng ở người ghép tạng đảm bảo cho liệu pháp ức chế chống virus. Trên các bệnh nhân nhiễm HIV, liệu pháp chống virus thường không đòi hỏi có mặt triệu chứng lâm sàng.
Bệnh CMV tiên phát ở đường tiêu hóa trên các bệnh nhân ghép tạng đặc khó điều trị và có thể tái phát. Tỷ lệ tái phát gần đây nghiên cứu trên nhóm người ghép tạng đặc sau điều trị nhiễm trùng CMV tại Mayo clinic. Các nàh điều tra tìm thấy có liên quan đến hệ thống tiêu hóa là có ý nghĩa với tình trạng tái phát với CMV nhưng nội soi tiêu hóa không cần thiết phiên giải sang giảm nguy cơ tái phát CMV(?).
Đồng nhiễm virus HIV và virus Cytomegalovirus
CMV thường được phân lập trên các bệnh nhân đồng nhiễm với các loại vi khuản, víu, ký sinh trùng và các nhân nấm khác. Thực tế, CMV có thể tìm thấy trong phổi khoảng 75% cá nhân nhiễm cả HIV và Pneumocystis.Nhiễm trùng CMV trong viêm phổi Pneumocystis chưa rõ ràng, và điều trị sau đó thường dẫn đến viêm phổi và thiếu khí, nghĩa là điều trị CMV không phải đều hiệu quả trên tất cả ca bệnh. Vì không biết lý do, nên viêm phổi do CMV không có đồng nhiễm vẫn không biết.
Trên các bệnh nhân nhiễm HIV, thì CMV liên quan đến toàn bộ đường tiêu hóa. Trong đường tiêu hóa trên, CMV đã được phân lập từ các vét loét thực quản và loét tá tràng. Các bẹnh nhân có bênh lý tiêu hóa trên có thể có triệu chứng đau và khó nuốt. Các bênh nhân bị CMV ở đường tiêu hóa dưới có thể biểu hiện tiêu chảy (viêm đại tràng). Viêm đại tràng do CMV thường ảnh hưởng chỉ đại tràng phải, cần thiết nội soi toàn bộ và sinh thiết nhiều chỗ để cho chẩn đoán chính xác. Chẩn đoán bệnh lý tiêu hóa do CMV lệ thuộc vào mẫu bệnh phẩm sinh thiết.
Sự phục hồi của các CMV trong các nuôi cấy mô có thể giúp nhưng khó phiên giải kết quả vì CMV ẩn cư. CMV có thể phân lập taij nhiều vùng khác nhau không nhất thiết liên quan đến bệnh, do vậy cần làm thêm xét nghiệm mô học.
Viêm võng mạc là một đặc điểm lâm sàng hay gặp của bệnh CMV trên một số bệnh nhân có HIV (+). Chúng xảy ra thường trên các bệnh nhân có lượng CD4 < 50 cells/µL, với tỷ lệ lên đến 40% trong quần thể này. Các bệnh nhân bị ảnh hưởng báo cáo có giảm lượng virus, …Trong nhiều trường hợp, bệnh tiến triển liên quan đến 2 bên mắt và thường kèm với bệnh do CMV hệ thống cơ quan. Bệnh CMV, khám mắt cho thấy nhiều vùng vàng trắng với xuất tiết quanh mạch. Xuất huyết hiện diện và thường liên đới đến hình ảnh "cottage cheese and ketchup". Các thương tổn có thể xuất hiện tại vùng ngoại vi của đáy mắt, nhưng chúng tiến triển trung tâm.
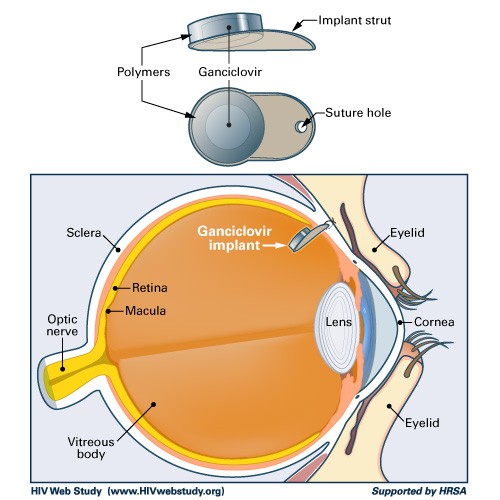
Ganciclovir đã được dùng điều trị bệnh võng mạc CMV. Tiếc thay, nó chỉ diễn tiến bệnh chậm rãi. Nhiều thầy thuốc lâm sàng đã chuyển sang dùng Foscarnet sau khi Ganciclovir thất bại. Ganciclovir từ lâu là một liệu pháp quan trọng trong quản lý và trị liệu cho bệnh lý võng mạc do CMV. Lựa chọn điều trị tối ưu gồm có thuốc Ganciclovir đưa vào thủy tinh thể, kèm theo dùng Ganciclovir đường toàn thân. Dùng Ganciclovir đường uống có thể dùng để dự phòng viêm võng mạc CMV nhưng không nên dùng để điều trị. Tỷ lệ viêm võng mạc CMV đã giảm xuống đáng kể kể từ khi dùng các thuốc chống virus có hoạt tính cao. Trong quá trình cải tiến lại đáp ứng miễn dịch trên bệnh nhân có HIV (+) và dùng liệu pháp chống virus, viêm võng mạc có thể bị xấu đi một thời gian. Nếu viêm nhiễm nặng xảy ra, điều trị thuốc corticosteroid là cần thiết.
Trên các bệnh nhân có HIV (+), CMV có thể gây ra bệnh lý ở hệ thần kinh trung ương và ngoại biên.
Khám xét lâm sàng tổng thể
Khám thực thể
Hầu hết các bệnh nhân nhiễm CMV biểu hiện một số triệu chứng lâm sàng khi khám:
- Nhiễm CMV tiên phát có thể là một nguyên nhân của sốt không rõ nguyên nhân;
- Khi xuất hiện triệu chứng, phát triển 9-60 ngày kể từ khi nhiễm trùng tiên phát;
- Có thể phát hiện tình trạng viêm hầu họng;
- Khám phổi có thể phát hiện nhiều ran nổ êm dịu;
- Hạch lympho và lách có thể lớn, vì thế CMV nên được chú trọng trong chẩn đoán phân biệt các bệnh nhiễm trùng với bệnh lý hạch lympho;
- Nhiều thầy thuốc tin rằng bệnh nhiễm bạch cầu đơn nhân CMV là ít có liên quan đến viêm hầu họng và bệnh lý hạch cổ hơn là nhiễm virus bạch cầu đơn nhân Epstein Barr (EBV). Một nghiên cứu gần đây trên các trẻ em nhỏ đặt ra câu hỏi về tính chính xác của các hình ảnh lâm sàng này;
- Nghiên cứu còn tìm thấy rằng bệnh lý hạch tuyến cổ thường gặp trên các bệnh bạch cầu đơn nhân loại EBV hơn là bệnh nhân nhiễm bạch cầu đơn nhân CMV (83% vs.75%). Mặc dù không có ý nghĩa về mặt thống kê, song dựa vào dầu hiệu này để phân biệt bệnh lý bạch cầu đơn nhân (mononucleosis) do CMV và EBV là khó.
Xét nghiệm cận lâm sàng
Cytomegalovirus (CMV) đã được phát hiện trên nuôi cấy (nguyên bào sợi ở người), huyết thanh học và thử nghiệm kháng nguyên, PCR và phân tích tế bào học. Nồng độ IgM tăng trên các bệnh nhân có nhiễm CMV gần đây, hoặc có tăng gấp 4 lần nồng độ và hiệu giá kháng thể IgG. Kết quả CMV IgM dương tính giả có thể nhìn thấy trên các bệnh nhân nhiễm EBV hoặc HHV-6, cũng như trên các bệnh nhân có nồng độ yếu tố thấp (RF) cao.
Một số thử nghiệm nhạy đủ để phát hiện kháng thể kháng CMV IgM sớm trong giai đoạn đầu của bệnh (kháng nguyên nhân CMV sớm, kháng nguyên CMV virus capsid) và trong khi có sự tái hoạt của CMV. Khi nhiễm EBV, quan sát thấy sự tái hoạt virus với một kết quả IgM (+) trong sự hiện diện của kháng thể IgG là không thường gặp. Điều này hay nhìn thấy nhất trong nhiễm trùng tái đi tái lại trên các bệnh nhân suy giảm miễn dịch;
Một loại xét nghiệm kháng thể đơn dòng với kháng nguyên sớm qua trung gian chống lại CMV hiện đang sẵn có. Phản ứng này với protein sớm và có thể phát hiện nhiễm CMV 3 giờ trong khi nhiễm. Nhuộm thấy đậm độ của hạt nội nhân đáng chú ý. Các hình thức nhuộm nhân khác khác hoặc bào tương đều chưa cụ thể. Trên các quần thể ghép tạng, thử nghiệm kháng nguyên hoặc PCR được dùng đến (đôi khi cùng với xét nghiệm tế bào học) để xác định chẩn đoán và điều trị.
Các xét nghiệm kháng nguyên (Antigen testing)
- Kháng nguyên trong máu được xác định khi phát hiện được kháng nguyên CMV pp65 trong bạch cầu;
- Thử nghiệm pp65 dùng phát hiện thông tin protein cơ chất trên virus CMV, hoặc làm thử nghiệm IFA hoặc khuyếch đại chuỗi RNA thông tin (messenger RNA amplification). Các loại protein này chỉ trình diện trong quá trình sao chép virus;
- Thử nghiệm kháng nguyên thường là các xét nghiệm cơ bản của các viện trong vấn đề trị liệu thuốc chống virus ở các đối tượng ghép tạng và có thể cho phép phát hiện bệnh lý ẩn lâm sàng trên nhóm bệnh nhân có nguy cơ cao. Thử nghiệm có độ nhạy và đặc hiệu lại cho kết quả nhanh;
- Thử nghiệm kháng nguyên không thể sử dụng trên các bệnh nhân có giảm bạch cầu, vì các test này phát hiên kháng nguyên trong bạch cầu neutrophils;
- Trên những bệnh nhân suy giảm miễn dịch, kháng nguyên trong máu CMV mức độ nhẹ hoặc trung bình có thể chỉ ra sự tái hoạt hoặc nhiễm trùng CMV;
- Người ta đã báo cáo thử nghiệm kháng nguyên pp65 và phương pháp CMV PCR định lượng (COBAS Amplicor Monitor Test) có hiệu quả trong chẩn đoán và giám sát các bệnh nhân nhiễm CMV hoạt động.
Xét nghiệm PCR định tính(Qualitative polymerase chain reaction).
- PCR định tính (Qualitative PCR) được dùng để phát hiện CMV trong máu và các mẫu bệnh phảm là mô;
- PCR lệ thuộc vào quá trình sao chép các cặp mồi đặc hiệu cho vị trí gen CMV. Các đoi mồi thường gắn với vùng của virus mã hóa cho các kháng nguyên sớm;
- PCR định tính rất nhạy, nhưng vì CMV DNA có thể phát hiện trên các bệnh nhân có hay không có bệnh hoạt động, tính thiết thực về mặt lâm sàng của PCR định tính có giới hạn của nó. Serial PCR có thể giúp ích cho lâm sàng hơn;
- Lợi ích của kết quả dương tính trước khi có kháng nguyên trong máu trên những bệnh nhân ghép tạng mang virus máu;
- Kết quả âm tính chỉ ra các bệnh nhân không có virus CMV trong máu;
- Trên những bệnh nhân ghép tạng, kết quả PCR âm tính cho biết sự tái hoạt nhưng không nhiễm trùng.
Xét nghiệm PCR định lượng (Quantitative polymerase chain reaction)
- PCR định lượng (Quantitative PCR) đã được dùng để phát hiện CMV trong huyết tương. Lợi điểm của PCR định lượng hơn hẳn PCR thường. Một cách lý tưởng, PCR định lượng có độ nhạy như PCR định tính và cung cấp ước tính số gen nhiễm hiện diện trong huyết tương;
- Một nghiên cứu hơn 3400 mẫu máu từ các bệnh nhân ghép tạng xét nghiệm CMV PCR và thử nghiệm kháng nguyên pp65 trong máu tìm thấy RT-PCR đối với CMV DNA có thể dùng thay cho kháng nguyên trong máu trong việc giám sát nhiễm CMV và xác định khi điều trị ưu tiên;
- Về mặt lý thuyết, lượng virus CMV sẽ chỉ ra liệu trình trị liệu cần thiết vì các bệnh nhân có lượng virus thấp dưới sẽ không phát triển thành bệnh CMV. Tuy nhiên, mức độ virus trong máu cần thiết xác đinh bệnh xảy ra có thể khác nhau tùy thuộc vào các yếu tố vật chủ và loại tạng ghép, và điều này cần xác định một cách thận trọng. Chẳng hạn, trên những viêm võng mạc do CMV, lượng virus có giá trị tiên đoán dương kém, có nghĩa là tính thống nhất về lâm sàng kém. Lượng virus CMV có thể phát hiện được vào thời điểm viêm võng mạc do CMV chẩn đoán chỉ ra một liên quan tăng tỷ lệ tử vong (P = 0.007).Liên quan CMV ở đường tiêu hóa cũng có liên quan không nhiều đến virus CMV trong máu ;
- Xét nghiệm PCR gồm có COBAS Amplicor CMV Monitor test (chỉ dùng trong nghiên cứu tại la bô), và Hybrid Capture System CMV DNA test dùng định lượng, qualitative Hybrid Capture test (FDA chấp nhận). Vì lượng virus không thể so sánh trong số các thử nghiệm khác nhau, điều quan trọng là sử dụng các thử nghiệm giống nhau trên cùng loại mẫu bệnh phẩm (máu hoặc huyết tương) khi giám sát bệnh nhân theo thời gian theo dõi.
Thử nghiệm trong vỏ (Shell vial assay)
- Thử nghiêm trong vỏ (SVA) được thực hiện bằng cách thêm các mẫu bệnh phẩm lâm sàng vào trong một lọ nhỏ chứa các dòng tế bào cho phép với CMV. Các lọ này được đem ly tâm tốc độ thấp và đặt vào trong tủ ấm. Sau 24 và 48 giờ, môi trường nuôi cấy mô bị loại khỏi và lấy các tế bào nhuộm sử dụng chất
đánh dấu huỳnh quang kháng thể chống CMV. Các tế bào này đọc thông qua kính hiển vi huỳnh quang. Cũng có thể các tế bào nhuộm với kháng thể chống lại CMV, theo đó bởi một loại Ig miễn dịch đánh dấu huỳnh quang;
- Thử nghiệm này cho độ nhạy như phương pháp nuôi cấy mô.
Xét nghiệm tế bào
Kể cả nghiên cứu nội bào bao quanh bởi một vòng halo rõ ràng cho thấy nhiều chủng khác nhau (nhuộm Giemsa, Wright, hematoxylin-eosin, Papanicolaou). Điều này cho thấy sự hiện diện hình ảnh mắt cú đặc trưng ("owl's eye").
Chẩn đoán hình ảnh
Việc chẩn đoán viêm phổi do CMV có thể đề nghị chụp phim phổi, nhưng phương pháp chẩn đoán này không thể chẩn đoán phân biệt giữa chúng với các nguyên nhân gây viêm phổi khác trên các vật chủ suy giảm miễn dịch. Chụpphim phổi cho hình ảnh viêm phổi và một kết quả BAL đó là CMV (+) có thể giúp ích cho chẩn đoán.
CT scan có thể là một phương pháp chẩn đoán nhạy hơn cho thâm nhiễm phổi. Chúng óc giá trị trên các bệnh nhân thiếu khí và không thâm nhiễm trên hình ảnh chụp phim phổi bằng X- quang.
Một số khám nghiệm khác
Thử nghiệm kháng với Cytomegalovirus (CMV resistance testing)
Nhiễm trùng CMV tiếp tục cho thấy một vấn đề y tế quan trọng trên nhóm bệnh nhânghép tạng và kháng thuốc virus đang là vấn đề đối mặt. Trên các cá nhân ghép tạng đặc, kháng thuốc ganciclovir tìm thấy chủ yếu trên số người cho tạng dương tính, phổi thận âm tính/ người nhận ghép tụy âm tính. Trong số bệnh nhân ghép tế bào gốc, kháng đầu tiên ảnh hưởng lên những người “donor-negative, recipient-positive group”. Các yếu tố nguy cơ khác gồm giáng hóa tế bào T, dùng liệu pháp thuốc chống virus hơn 3 tháng, lượng virus trong người cao, bệnh CMV tái phát, tăng nồng độ ức chế miễn dịch, nồng độ thuốc chống víu dưới liều tối ưu do không phối hợp tốt của bệnh nhân hoặc giảm hấp thu thuốc. Kháng với Foscarnet và Cidofovir đã được báo cáo trên những người ghép tế bào gốc và tạng đặc.
Quá trình hình thành kháng thuốc phải mất vài tuần đến vài tháng. Thực tế, trong số những bênh nhân nhiễm HIV, có một tỷ lệ 10% kháng thuốc Ganciclovir đã được báo cáo ở thời điểm 3 tháng. Kháng thuốc nên nghi ngờ để chẩn đoán trên các bệnh nhân đáp ứng ban đầu với liệu pháp điều trị CMV nhưng sau đó lại hình thành phát sinh kháng biểu hiện tăng lượng virus dù thuốc vẫn đủ. Và chúng ta cũng nên cân nhắc và xem xét trên các đối tượng có suy sụp và triệu chứng lâm sàng nặng hơn.
Chỉ có hai gen kháng CMV đã được báo cáo qua ghi nhận đến ngày nay: UL-97 và UL-54. UL-97 (một gen phosphotransferase), mã hóa kháng cho Ganciclovir, trong khi đó đột biến UL-54 (viral DNA polymerase) lại thiên về kháng với Ganciclovir, Foscarnet, Cidofovir. Khoảng 90% số bệnh nhân, kháng Ganciclovir khởi đầu từ đột biến UL-97. Đến nay, đột biến kháng Ganciclovir đã chúng minh trên UL-97 tìm thấy chỉ tại vị trí codon 460, 520 và 590-607. Đột biến tại codons 696-850 trung gian cho kháng Foscarnet, đột biến tại các vị trí này không thường kahngs chéo với các thuốc kháng chống CMV. Nếu một bệnh nhân hình thành kháng khi dùng Cidofovir, nó có thể gây ra bởi đột biến kháng UL-54, điều này sẽ mã hóa cho kháng chéo với Ganciclovir.
Các thử nghiệm đặc biệt có thể dùng để kiểm tra kháng. Phương pháp dùng phổ biến và rộng rãi nhất là một loại thử nghiệm phân tích về kiểu gen sử dụng mẫu bệnh phẩm là dịch (dịch não tủy, máu) chứa CMV DNA hoặc các mẫu nuôi cấy dương tính với CMV. Kết quả xét nghiệm kiểu gen có thể thực hiện và kết quả nhận trong vài ngày. Tiếc thay, thử nghiệm này đắt tiền và có thể không thích hợp cho vấn đề đột biến. Do đó, làm quen với kỹ thuật và phiên giải kết quả là khâu quan trọng nhất.
Các thử nghiệm đánh giá kháng khác gồm đo lường lượng virus qua xác định định lượng DNA hoặc lượng kháng nguyên trong máu cũng như thử nghiệm “phenotypic plaque reduction assay”. Vấn đề trước chưa chuẩn hóa tốt và sự phiên giải có thể khác nhau từ viên này đến viện khác. Ngoài ra, trong một số bệnh do CMV (như viêm võng mạc), xét nghiệm lượng virus cho giá trị tiên đoán dương tính (PPV) thấp. Phương pháp “ plaque reduction assay” mất ít nhất 1 tháng mới hoàn chỉnh, chuẩn hóa nghèo nàn và không thể thực hiện thường quy tại la bô.
Xét nghiệm về mô học
Điểm đặc trưng của quá trình nhiễm trùng CMV tìm thấy trong nhân bao gồm cả nhiễm virus Herpes. Nhiễm trùng CMV có thể xác định qua xét nghiệm lai tại chỗ hoặc nhuộm gián tiếp hay trực tiếp nội nhân qua cách sử dụng các kháng thể đặc hiệu CMV liên kết vowiss một hệ thống chỉ điểm (như nhuộm horseradish peroxidase, fluorescein).
Thái độ xử trí /chăm sóc y khoa (Medical Care)
Lựa chọn tốt nhất cho điều trị và dự phòng bệnh do CMV vẫn là ganciclovir và valganciclovir. Các lựa chọn khác được liệt kê dưới đây như lựa chọn “second-line” (foscarnet hoặc cidofovir) hoặc sử dụng dạng “off-label” (leflunomide). Không có sự thống nhất vào lúc này để dự phòng hay điều trị ưu tiên trước là tiếp cận tốt nhất trong dự phòng nhiễm CMV trên các bệnh nhân là người ghép tạng đặc.
Tỷ lệ mắc bệnh do CMV giảm đi đáng kể trên những người ghép tạng đặc kể từ khi có sự phát triển của các liệu pháp thuốc chống virus đặc hiệu. Để bảo vệ lâu dài chống lại bệnh CMV, bệnh nhân cần phải phát triển một đáp ứng miễn dịch chống CMV đặc hiệu.
Điều trị bằng Ganciclovir
- Đây là thuốc lựa chọn để điều trị bệnh lý do CMV đường tĩnh mạch Ganciclovir, dù valganciclovir có thể dùng điều trị CMV trên một số ca lựa chọn lọc;
- Ganciclovir là một đồng phân nucleoside có thể ức chế tổng hợp DNA cùng một phương cách như Acyclovir. Điểm khác biệt chính là CMV không chứa một thymidine kinase;
- Protein UL97 phosphorylates hóa ganciclovir với ganciclovir monophosphate. Một trong những cơ chế kháng Ganciclovir là một sự thay đổi trên UL97. Đột biến tại codon 460 và 520 và các đột biến hoặc mất đoạn khoảng codons 590-596 trên UL97 gây ra hầu hết khángGanciclovir, dù các cơ chế kháng khác đã được trình bày;
- Ganciclovir có hoạt tính chống lại CMV, HSV, VZV, HHV-6, HHV-7, HHV-8. Tuy nhiên, một loại đồng phân nucleoside khác (như Famciclovir, Penciclovir, Acyclovir) có ưu thế trong sử dụng điều trị VZV và nhiễm trùngHerpes simplex;
- Tác dụng phụ quan trọng nhất của Ganciclovir gồm có sốt, phát ban và tiêu chảy và xuất huyết (giảm bạch cầu, thiếu máu và giảm tiểu cầu). Giảm bạch cầu được quản lý thông qua giảm liều và/ hoặc thêm các yếu tố phát triển (như granulocyte colony-stimulating factor [G-CSF], granulocyte-macrophage colony-stimulating factor [GM-CSF]);
- Dùng Ganciclovir đường uống có nồng độ trong huyết thanh thấp hơn gấp 5-10 lần dùng tĩnh mạch Ganciclovir. Valganciclovir hydrochloride, một phiên bản đường uống của (L-valyl ester) Ganciclovir, đã được chấp nhận dùng điều trị viêm võng mạc mắt do CMV trên các bệnh nhân nhiễm HIV;
- Một thử nghiệm ngẫu nhiên trên các bệnh nhân viêm võng mạc do CMV cho thấy dùng Valganciclovir đường uống có hiệu qủa tương đương dùng Ganciclovir đường tĩnh mạch khi dùng chúng như liệu pháp điều trị ưu tiên. Mặc dù không có thử nghiệm so sánh với valganciclovir đường uống như một liệu pháp duy trì, song các nghiên cứu về dược động học cho thấy Valganciclovir có hiệu quả như là Ganciclovir đường tĩnh mạch;
- Trong điều trị viêm phổi do CMV, Ganciclovir được chỉ định cùng với CMV-specific immune globulin. Tuy nhiên, người ta vẫn chưa biết Ganciclovir hỗ trợ về mặt miễn dịch như thế nào với immune globulin. Vì thế, nó dẫn đến hiệu quả tốt hơn trong điều trị viêm phổi do CMV;
- Thời gian trị liệu có khác nhau. Một số thầy thuốc lâm sàng có chỉ định dùng Ganciclovir dài đến 2-4 tuần, lệ thuộc vào tình trạng lâm sàng của bệnh nhân. Gần đây, các nàh điều tra đã nghiên cứu liệu trình dùng ngắn hơn liệu pháp Ganciclovir đường tĩnh mạch trong điều trị nhiễm hoặc bệnh do CMV. Nếu hiệu quả, điều này có thể giúp cải thiện chất lượng sống cho bệnh nhân để giảm thời gian nằm viện;
- Cách sử dụng khác của Ganciclovir gồm điều trị thể bệnh tiêu hóa trên các đối tượng ghép tạng có HIV (+). Ganciclovir cũng đã dùng điều trị viêm thực quản do CMV trên các quần thể bệnh nhân;
- Thuốc cũng được dùng điều trị tiêu chảy thứ phát sau viêm đại tràng hoặc viêm ruột trên những bệnh nhân HIV (+) sau khi sinh thiết và xác định bệnh CMV. Vì khả năng tái phát bệnh CMV cao (50%), nên dùng thuốc duy trì nên được khuyên cho tất cả bệnh nhân;
- Ganciclovir cũng được sử dụng để điều trị bệnh lý thần kinh trung ương do CMV, gồm cả viêm não và bệnh lý rễ thần kinh.
Điều trị bằng Valganciclovir
- Valganciclovir là một “prodrug” của Ganciclovir hoạt hóa trong ruột và trong gan đối với Ganciclovir;
- Valganciclovir có sinh khả dụng là 60%. Valganciclovir 900 mg dùng đường uống 1 lần./ngày tương đương 1 lần/ ngày đường tĩnh mạch Ganciclovir 5 mg/kg;
- Một nghiên cứu phân tihcs tổng hợp (meta-analysis) chỉ ra hiệu lực tương đương giữa 900 mg valganciclovir và 450mg trong điều trị dự phòng nhiễm CMV trên các bệnh nhân ghép tạng, dù liều 900 mg mỗi ngày có liên quan tăng nguy cơ gấp 3 lần giảm bạch cầu và 2 lần tăng nguy cơ thải ghép tạng;
- Valganciclovir được dùng để điều trị các trường hợp CMV chọn lọc. Hầu hết kinh nghiệm coh thấy trên những người ghép tụy và thận và bệnh nhân HIV/AIDS có viêm võng mạc do CMV đã được thiết lập điều trị;
- Thuốc cũng được dùng điều trị trước tiên hoặc phổ cập dự phòng CMV;
- Tỷ lệ lọc cầu thận (glomerular filtration rate_GFR) < 10 là một chống chỉ định dùng Valganciclovir use.
Dự phòng bằng Ganciclovir
- Một sử dụng thành công của Ganciclovir dùng để dự phòng và điều trị trước đối với bệnh CMV trên các bệnh nhân ghép tạng. Không có điều trị dự phòng CMV, 30%-75% só người ghép tạng đã nhiễm CMV, 8%-30% phát triển thành bệnh CMV;
- Dùng Ganciclovir đường uống thay thế cho Valganciclovir để dự phòng và điều trị “preemptive” vì tính sinh khả học;
- Dự phòng được chỉ định cho tất cqar bệnh nhân có huyết thanh CMV (+). Điều trị “preemptive” cho các bệnh nhân có bằng chứng virus đang sao chép. Xét nghiệm nuôi cấy máu dương tính, kháng nguyên pp65 (+) trong máu, PCT cho CMV sử dụng marker đối với trị liệu ban đầu. Cả hai loại tiếp cận dự phòng và điều trị trước đã được sử dụng, và cả hai đã cho thấy giảm bệnh CMV trên các bệnh nhân ghép tủy xương và tạng đặc. Lựa chọn liệu pháp hoặc phác đồ thích hợp có thể xác định bởi tác dụng ngoại ý của thuốc và khả năng kiểm tra về mặt vi sinh của nơi đó. Dự phòng phổ biến so với điều trị trước (Universal prophylaxis versus preemptive therapy) như là tiếp cận tốt nhất vẫn còn là vấn đề bàn cãi và khác nhau giữa các viện;
- Điều trị ưu tiên trước là rất hấp dẫn vì giới hạn sử dụng của thuốc Ganciclovir
đối với một quần thể chọn lọc có nguy cơ cao với bệnh CMV, loại thải độc tính trên hầu hết bệnh nhân không được xác định là bệnh CMV, giảm chi phí chăm sóc y tế;
- Một nghiên cứu so sánh trên 96 bệnh nhân ghép thận ở Ý từ tháng 5.2006 đến tháng 12.2007, tất cả họ nhận điều trị trước bằng Ganciclovir và/ hoặc Valganciclovir, với 100 bệnh nhân chứng nhận thuốc sự phòng bệnh CMV. Một loạt định lượng virus làm hàng tuần để đánh giá trong suốt 4 tháng đầu tiên. Những bệnh nhân không có triệu chứng lựơng DNA đánh giá virus > 100.000 copies/mL xác đinh bằng PCR, được điều trị trong 3 tháng bằng hoặc cho đến khi giải quyết xong tình trạng sao chép virus. Trong số 96 người ghép tạng, lượng virus CMV trong máu có tăng trong số 14 người không có triệu chứng đã được điều trị bằng Valganciclovir đường uống trong 3 tháng. Sau thời gian theo dõi trung bình 13.3 tháng, không có bệnh nhân nào trong số 14 ca trên phát triển thành bệnh CMV, dẫn đến cho các tác giả kết luận Valganciclovir dùng điều trị ưu tiên trước an toàn và hiệu quả trong ngăn ngừa bệnh do CMV;
- Ngược lại, một nghiên cứu về kháng nguyên trong máu loại CMV pp65 như là một điểm chốt trong điều trị cho thấy dự phòng có hiệu quả hơn điều trị trước tiên trong việc ngăn ngừa viêm phổi do CMV trên các đối tượng ghép tủy xương. Đồng thời, Ganciclovir lồng vào có liên quan đến nhiễm nấm xâm nhập sớm và bệnh CMV muộn;
- Một số chuyên gia tin rằng dự phòng CMV trên các cá nhân ghép tạn đặc có thể bảo vệ chống lại gián tiếp CMV hiệu quả không được đo lường bằng nồng độ, như thải ghép, nhiễm trùng cơ hội và bệnh lý mạch máu có liên quan đến ghép tạng;
- Tiếp cận dự phòng cũng nhìn thấy điểm thành công trong việc loại trừ bệnh do CMV; tuy nhiên, độc tính tăng lên cùng với vì bệnh nhân không óc tái hoạt virus có thể phơi nhiễm với một lượng thuốc chống virus. Nhiều trung tâm ghép tạng bảo tồn liệu pháp dự phòng đối với các bệnh nhân có nguy cơ (CMV-positive donors/CMV-negative recipients) đối với sự tái hoạt bệnh và sử dụng thử nghiệm kháng nguyên cho điều trị trước tiên trên các bệnh nhân khác;
- Một số chuyên gia khuyến cáo mở rộng thời gian dự phòng CMV để giảm ức chế miễn dịch. Họ cảm thấy điều này có thể bảo vệ các bệnh nhân khỏi bệnh lý CMV muộn;
- Sử dụng thuốc Ganciclovir kéo dài có liên quan đến quá trình hình thành kháng thuốc.
Điều trị bằng Foscarnet
- Foscarnet là một chất ức chế chuỗi DNA của quá trình phosphoryl hóa. Thuốc được dùng để điều trị HSV kháng thuốc và các virus kháng với Ganciclovir. Đây là một thuốc điều trị virus có hiệu quả;
- Thận trọng trên các bệnh nhân có vấn đề về chức năng thận. Các thay đổi nhỏ trong nồng độ creatinine đòi hỏi tính toán lại hệ số thanh thải thận. Foscarnet là một chất gây độc cho thận,bệnh nhân phải bổ sung nước;
- Foscarnet có thể gây chuyển hóa calcium và phosphorus. Các tác dụng ngoại ý khác gồm độc cho thận, thiếu máu, nhức đầu và buồn nôn. Thuốc có thể gây một phản ứng thuốc cố định trên dương vật;
- Foscarnet không đòi hỏi quá trình phosphoryl hóa nội bào. Kháng thuốc Foscarnet là thứ phát đối với các đột biến của quá trình tổng hợp chuỗi DNA tại codon 696-845.
Dự phòng bằng Acyclovir
- Liều cao thuốc valacyclovir, penciclovir, famciclovir, acyclovir đã được dùng dự phòng ch cho bệnh do CMV trên những cá nhân ghép tạng. Kết quả về hiệu quả thay đổi tùy thuộc vào quần thể bệnh nhân ghép;
- Nhóm ghép tạng châu Âu có thể dùng nhiều acyclovir hoặc valacyclovir để dự phòng bệnh do CMV hơn là nhóm ở Mỹ;
- Thử nghiệm In vitro chỉ ra cho thấy một số chủng CMV có thể nhạy với Acyclovir;
- Nhìn chung, dự phòng bằng acyclovir prophylaxis không hiệu quả như dự phòng bằng ganciclovir.
Dự phòng bằng Cidofovir
- Cidofovir là một nucleotide ức chế sự sao chép DNA;
- Thuốc có hiệu quả chống lại nhiều loại virus, thuốc cũng được dùng điều trị viêm võng mạc do CMV khó trị trên các bệnh nhân nhiễm HIV;
- Kháng thuốc Ganciclovir không cần thiết sử dụng đến Cidofovir;
- Các bệnh nhân phải bù nước và thuốc phải chỉ định với probenecid để bảo vệ ống thân.
Leflunomide
- Leflunomide là một chất chuyển hóa dùng như một chất điều hòa bệnh trên các bệnh nhân viêm khớp dạng thấp;
- Thuốc cũng đã dùng thành công trong cả ddieuf trị và dự phòng bệnh do CMV;
- Thất bại thuốc Leflunomide đã được báo cáo trên những đối tượng ghép tế bào gốc tăng tái tạo máu.
Dùng globuline miễn dịch cho CMV (Cytomegalovirus immune globulin)
- Các globuline miễn dịch CMV đã được chấp thuận bởi cơ quan FDA để dự phòng bệnh lý CMV trên các người ghép tạng phổi có nguy cơ cao khi cho dùng Ganciclovir. Trong một nghiên cứu hồi cứu về người ghép “cardiothoracic”, dùng CMV immune globulin cùng với Ganciclovir đã cho tỷ lệ không có bệnh cao hơn đối với CMV, thải mảnh ghép ít hơn, tỷ lệ sống sót cao hơn, giảm độ dày màng mạch trong của mạch vành (CIT_coronary intimal thickening) so với các bệnh nhân dùng Ganciclovir đơn thuần. Nghiên cứu ngẫu nhiên tiến cứu đòi hỏi phải thực hiện để xác định cho kết quảnghiên cứu này;
- CMV Ig được dùng phối hợp với Ganciclovir để điều trị viêm phổi do CMV;
Chăm sóc bệnh nhân nội trú
- Các bệnh nhân nhiễm CMV phải được bù nước tốt hay hydrate hóa;
- Dinh dưỡng là yếu tố quan trọng vì nhiều bệnh nhân đã bị yếu sức do ghép hoặc nhiễm HIV;
- Với bất kỳ bệnh nhân nào, cần chú ý tránh vấn đề nhiễm trùng;
- Các bệnh nhân có bệnh do CMV mà bị suy giảm miễn dịch, có nghĩa là có nguy cơ cao nhiễm vi khuẩn hoặc nấm. Nếu có thể, thì nồng độ ức chế miễn dịch phải thấp.
Biện pháp chống dịch & Kiểm dịch biên giới:
- Không có quy định về kiểm dịch biên giới;
- Cách ly người bệnh. Các loại vaccine đang trong giai đoạn tửh nghiệm.
Tài liệu tham khảo
1. Bộ Y tế (2009). Cục Y tế dự phòng và môi trường. Cẩm nang phòng chống bệnh truyền nhiễm. Bệnh do virus Cytomegalovirus, trang 412 -415. NXBYH, Hà Nội 2009
2. Ryan KJ, Ray CG (editors) (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. pp. 556; 566–9. ISBN 0838585299.
3. Koichi Yamanishi; Arvin, Ann M.; Gabriella Campadelli-Fiume; Edward Mocarski; Moore, Patrick; Roizman, Bernard; Whitley, Richard (2007). Human herpesviruses: biology, therapy, and immunoprophylaxis. Cambridge, UK: Cambridge University Press. ISBN 0-521-82714-0.
4. Offermanns S, Rosenthal W (2008). Encyclopedia of Molecular Pharmacology. Springer. pp. 437–438. ISBN 978-3-540-38916-3.
5. Staras SA, Dollard SC, Radford KW, Flanders WD, Pass RF, Cannon MJ (November 2006). "Seroprevalence of cytomegalovirus infection in the United States, 1988–1994". Clin. Infect. Dis. 43 (9): 1143–51.
6. Caruso C, Buffa S, Candore G, et al. (2009). "Mechanisms of immunosenescence". Immun Ageing 6: 10. doi:10.1186/1742-4933-6-10.PMC 2723084.
|







 Trả lời kèm Trích dẫn
Trả lời kèm Trích dẫn